卡梅德生物科技(天津)有限公司
6 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
卡梅德生物科技(天津)有限公司
入驻年限:6 年
- 联系人:
卡梅德-小智
- 所在地区:
天津 武清区
- 业务范围:
抗体、技术服务、体外诊断、原辅料包材、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
![科研级Tefibazumab(替非组单抗) Anti-Fibrin-binding Surface Epitope Clumping Factor A重组抗体 Fibrin-binding surface epitope clumping factor A[Staphylococcus aureus]参照抗体](https://img1.dxycdn.com/p/s14/2025/0725/806/0044791190482468491.jpg!wh200)
科研级Tefibazumab(替非组单抗) Anti-Fibrin-binding Surface Epitope Clumping Factor A重组抗体 Fibrin-binding surface epitope clumping factor A[Staphylococcus aureus]参照抗体
品牌:卡梅德/KMD Bioscience
¥500 - 3200
咨询
科研级Vedolizumab(维多组单抗) Anti-ITGA4 & ITGB7重组抗体 ITGA4 & ITGB7参照抗体
品牌:卡梅德/KMD Bioscience
¥500 - 3200
咨询公司新闻/正文
CD47抗体开发技术路线汇总&分析
775 人阅读发布时间:2022-06-01 08:37
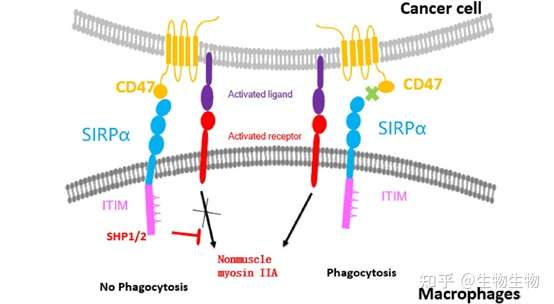
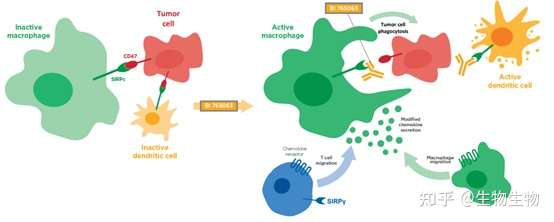
肿瘤细胞可以通过多种途径逃避机体免疫系统的识别和清除,如诱导免疫抑制的肿瘤微环境,降低肿瘤细胞的免疫原性等;其中,肿瘤细胞逃避天然免疫系统如巨噬细胞等吞噬细胞清除的机制之一是上调细胞表面“别吃我”(don't eat me)信号的表达。整合素相关蛋白(IAP,即CD47)便是一种重要的自我信号,它通过与巨噬细胞上的配体信号调节蛋白α(SIRPα)结合,进而抑制巨噬细胞对肿瘤细胞的吞噬;此外,在天然免疫细胞如树突状细胞等向适应性免疫T细递呈抗原的过程中,CD47也发挥着抑制作用。因此,CD47在肿瘤免疫中发挥着重要的调节作用,靶向CD47是一个潜在的抗肿瘤方向。
根据相关数据统计,目前已经有将近100种靶向CD47-SIRPα通路的药物正在开发中,包括单克隆抗体,融合蛋白,双特异抗体,ADC,小分子药物和CAR-T。其中以CD47单抗居多,其次为双特异抗体和融合蛋白。本篇文章我们解析一下目前相关药物的开发策略。
1
CD47单克隆抗体
靶向CD47的单克隆抗体目前主要分为三大类:
1)抗体不仅结合肿瘤细胞表面的CD47,而且也会结合红细胞和血小板表面的CD47。
这类抗体以Forty Seven的Hu5F9-G4为代表。为了避免Hu5F9-G4在治疗中因为结合红细胞而引起的血液毒性,Forty Seven临床设计中使用改良的给药方案,先给患者1 mg/kg的启动剂量(Priming dose)来触发体内老化红细胞的清除,虽然会导致暂时性轻度贫血,但同时可以刺激网织红细胞成熟分化产生新鲜的年轻红细胞。这些新生的红细胞表面表达“吃我”信号较低,对CD47抗体介导的吞噬作用不太敏感,因此可以承受后续Hu5F9 30 mg/kg的较高治疗剂量,并且实现充分的CD47受体占有率,发挥抗肿瘤作用。另外,因为这类抗体能够结合红细胞表面的CD47,所以在设计中一般都采用没有Fc相关作用的Ig4进一步降低副作用。因此理论上这类抗体仅能阻断CD47- SIRPα的相互作用,并且在临床中单药疗效有限,需要和其它抗体或者药物联合用药。
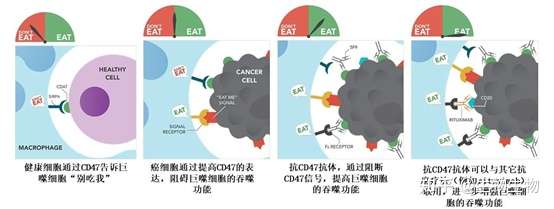
2) 第二类CD47单克隆抗体是通过特异性筛选获得的与红细胞不结合或者是微弱结合的抗体,这类抗体理论上具有较高的安全性,并且不需要通过改良临床给药方案降低相关血液毒性,以康方生物的AK117(Ligufalimab)和天境生物的TJC4(Lemzoparlimab)等为代表。
AK117(Ligufalimab)是由康方生物开发的靶向CD47的单克隆抗体,该抗体采用Ig4亚型并通过工程化最大限度降低Fc效应,并具有良好的血液学安全性和强大的促吞噬活性。在体外实验中,AK117区别于其他抗CD47抗体药物的差异化特征:食蟹猴贫血发生的影响很小,仅出现轻微的红细胞变化;对人血红细胞以及血小板的结合能力弱,不引起血小板毒性,同时不引起不引起红细胞聚集。在一期临床实验中,AK117最高给药队列为45mg/kg QW,各个剂量爬坡队列受试者中均未发生DLT(剂量限制性毒性)和未出现有临床意义的贫血,各队列受试者对药物耐受性良好,无需使用低剂量预激给药。受试者外周血T细胞的CD47的受体占有率(RO)在3mg/kg队列就已经达到并维持在100%。
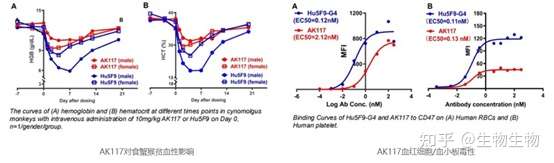
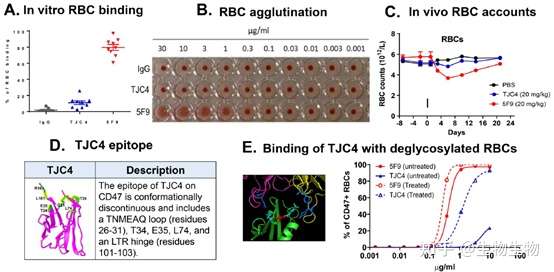
TJC4(Lemzoparlimab)是由天境生物开发的靶向CD47的单克隆抗体,该抗体同样为Ig4亚型的抗体。在筛选中,天境生物采用红细胞反筛选方法获得该抗体。和其他CD47抗体不同,TJC4能够识别独特的CD47抗原表位,而该表位在红细胞上由于糖基化修饰作用使得其不能充分暴露,从而导致TJC4对红细胞的结合力微弱。

TJC4 在美国进行的 I 期癌症临床研究试验结果显示,在没有任何预激给药的情况下,TJC4 每周单注射给药从 1mg/kg 至 30mg/kg 剂量范围内均显示出良好的耐受性,且在可评估患者中未观察到剂量限制性毒性或严重的血液学不良事件;在食蟹猴毒理实验中,在重复给药高达 100mg/kg 的高剂量下,都展现了良好的耐受性。
3)肿瘤微环境特异性激活抗体
第三类CD47单克隆抗体是通过技术手段使得抗体在血液中或者循环中不具有结合活性,当抗体进入肿瘤微环境中,在肿瘤中特异性酶的切割下,即可被切割暴露结合表位并激活其结合活性。这类抗体以天演生物的ADG153 SAFEbody 为代表。相关原理和数据这里不再赘述,详细分析见《天演药业条件激活性CD47抗体--ADG153 SAFEbody》
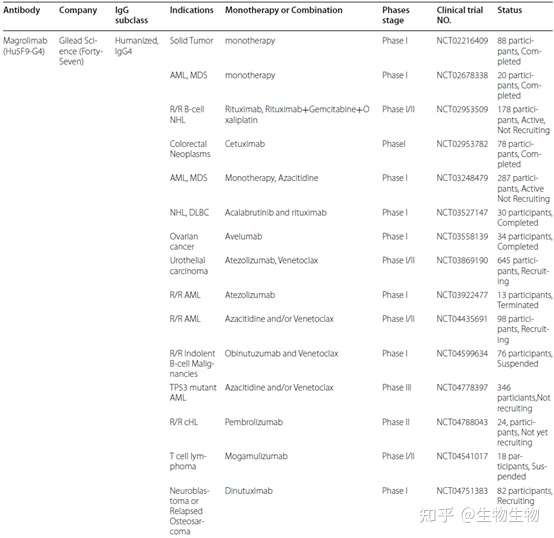
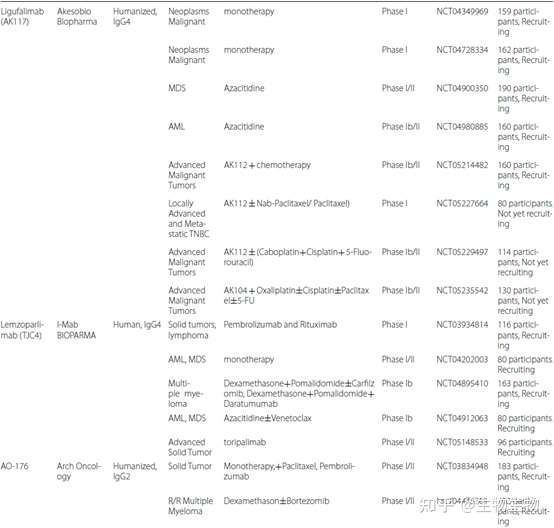
下表为CD47单克隆抗体开发相关管线

2
SIRP单抗
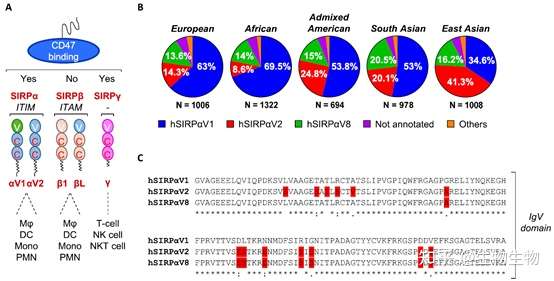
SIRPα的可变区在人体内含有10个等位基因,其中V1,V2和V8大约占据所有人种的90%,因此开发靶向SIRPα的抗体如果能同时结合V1,V2和V8,药物的药效理论上比靶向单一的V区药效更佳。除此之外,开发SIRPα还需要注意其它一些问题:
1)SIRPα表达在骨髓瘤细胞上,因此如果抗体不是靶向骨髓瘤细胞,抗体应该选择没有相关效应功能的Fc,这样可以避免抗体Fc介导的ADCC等效对免疫细胞进行杀伤。
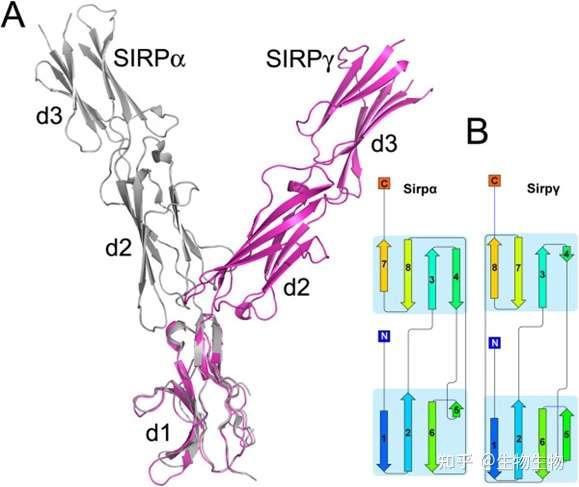
2)SIRPγ主要表达在T细胞和NK细胞上,其与CD47的结合能力低于SIRPα,T细胞上的SIRPγ和APC细胞上的CD47结合可以介导细胞与细胞的相互作用并增强抗原的呈递,最终导致T细胞增值和细胞因子的释放。SIRPγ和SIRPα具有74.37%的同源性,因此SIRPα抗体的开发应避免影响SIRPγ与CD47的相互作用。
3)在体内,抗原介导的抗体内吞可以导致抗体快速的降解,因此需要高剂量或者多次给药维持药物的水平
4)研究表明,靶向SIRPα抗体单药仅具有微弱或者几乎没有吞噬活性,但是其与其它药物如rituximab, cetuximab等联用时可以强烈的激活吞噬活性。
5)研究表明SIRPα在神经细胞中也有表达,因此临床中应注意神经毒性
靶向SIRPα的抗体目前多数位于临床早期,如BI765063,CC-95251和FSI-189。
BI765063是靶向V1和V2的单克隆抗体,其对V1具有较高的亲合力而对V2有较低的亲合力。I期剂量递增的数据表明,BI 765063单药或联合PD-1单抗BI 754091 (ezabenlimab) 治疗大量预处理晚期实体肿瘤患者具有良好的耐受性和活性(截至202106)。联合用药耐受性良好,无剂量限制毒性(DLTs),未达到最大耐受剂量(MTD)。在微卫星稳定(MSS)晚期子宫内膜或结直肠癌患者中,3例患者达到部分缓解(PR)。
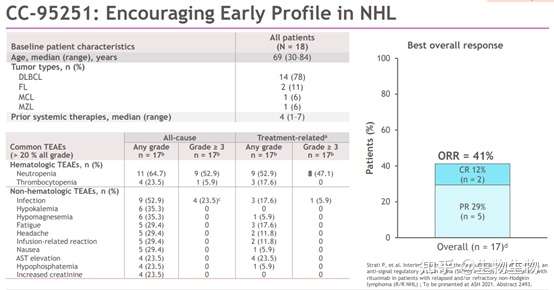
CC-95251是BMS开发的靶向SIRPα的单克隆抗体,目前该抗体的在SIRPα上的结合表位还没有披露。该抗体与Rituximab联合治疗在非霍奇金淋巴瘤的临床试验中已经表现出积极的活性和安全性,达到41%的客观缓解率。
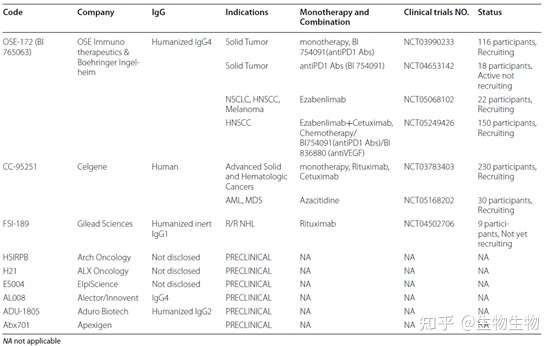
下表为目前在研的相关靶向SIRPα的单克隆抗体
3
SIRPα融合蛋白
SIRPα融合蛋白的开发利用了Trap的方式结合细胞表面的CD47,从而防止巨噬细胞上的SIRPα与CD47结合。目前该类药物主要是利用SIRPα的V区。部分公司选择SIRPαV1,另外一部分选择SIRPαV2进行药物开发,目前进入临床的主要有3家公司的4个药物,分别是Evorpacept(ALX148),TTI-621和TTI-622,和IMM01。
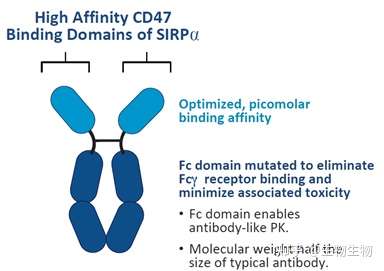
ALX148是由ALX Oncology开发的SIRPα V1D1-Fc融合蛋白,该蛋白对SIRPαV1D1进行突变(V6I, A271,I31F, E47V, K53R, E54S, H56P, L66T, V92I),改造后的SIRPαV1D1与野生型相比对CD47的亲合力提高了50000倍,同时该药物采用突变消除Fc的相关效应功能,进一步提高安全性。因此,虽然ALX148可以结合红细胞表面的CD47,但是其不会对红细胞造成损伤。另外,因为该药物本身不具有药效,因此临床中该药物主要是和其它药物联合用药,并且在一项与HER2抗体曲妥珠单抗(trastuzumab)及化疗联用的临床实验中,到达了72%的客观缓解率。除此之外,该药也与其它药物的联合疗法正在临床评估中(见下表)。
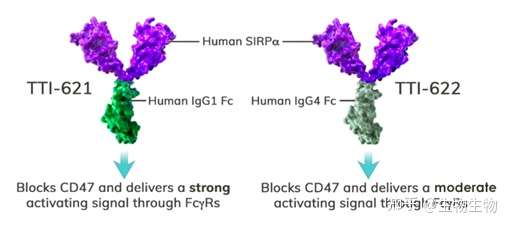
TTI-621和TTI-622是由TrilliumTherapeutics(已被辉瑞收购)开发的SIRPα V2D1-Fc融合蛋白,与ALX148不同,TTI-621和TTI-622采用了天然的SIRPαV2D1,该结构亚型可以高亲和力结合肿瘤细胞表面的CD47,但不结合红细胞表面的CD47,因此理论上具有更高的安全性。TTI-621采用具有相关Fc效应功能的IgG1亚型,而TTI-622采用不具有Fc相关效应功能的IgG4亚型。
但是在实际临床中,TTI-621因为血小板毒性因素问题,给药爬坡仅到2mg/kg剂量,在此剂量下T细胞表面CD47受体的占有率为60%。相比之下,TTI-622可以爬坡到18mg/kg的剂量,在不同治疗窗口下,TTI-622疗效与安全兼顾。另外,两者在临床中均观察到了贫血和血小板减少症,但是该症状一周之内会得到恢复。
目前这两个药物有多项临床正在进行中,既有单药治疗也有联合用药治疗。
IMM01是由宜明昂科开发的SIRPαV2D1-Fc融合蛋白,其在野生型的基础上进行了N80A突变,该突变主要是去除了糖基化,改善了PK,提高药物的生物利用度较高。因为SIRPαV2D1不结合红细胞的特性,因此其采用了含有Fc相关效应功能的IgG1亚型。
在临床中IMM01同样观察到了血小板减少症,但是在治疗后的24-48小时即可恢复,药效方面,IMM01在1.0 mg/kg的剂量下看到了药效,目前其单药用药正在临床评估中。
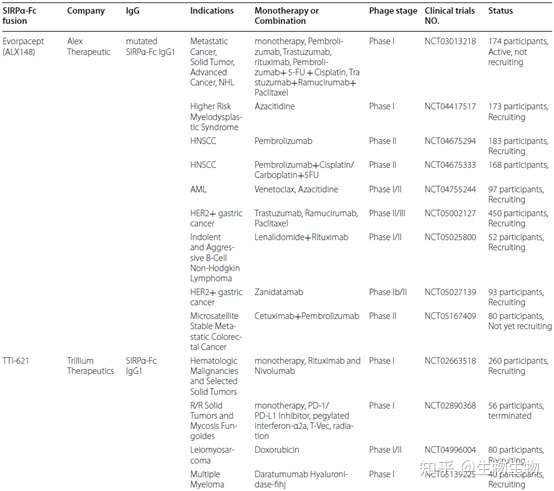
临床开发的SIRPα融合蛋白药物

4
双特异抗体
靶向CD47- SIRPα轴的双特异抗体从靶点结合方式上来看可以分为两大类:1)靶向CD47抗体的双特异抗体;2)融合有SIRPα的双功能抗体。
另外,靶向CD47- SIRPα轴的双特异抗体还可以根据其靶向的抗原进行分类,如靶向肿瘤抗原的双特异抗体(PD-L1, CD20,CD19, MSLN (Mesothelin), Claudin18.2, and Her2),);靶向免疫细胞的双特异抗体(PD-1, CD40, 41BB)及靶向细胞因子或者受体的双特异抗体(CSF-2 receptor/VEGF)等。不论以何种方式分类,靶向CD47- SIRPα轴的双抗大部分都是通过调节两个结合结构域的亲合力来降低对红细胞毒性,如相对降低靶向CD47的亲合力等。
PF-07257876是辉瑞开发的靶向CD47/PD-L1的双特异抗体,靶向这两个靶点的抗体也是国内开发较多的双特异抗体。PF-07257876设计中,为了防止CD47对红细胞等细胞的结合而引起严重的副反应,其采用了差异化的结合能力——抗体对PD-L1有高亲合力而对CD47有较低的亲合力,两者亲合力相差2个数量级以上(对PD-L1的亲合力为0.227 nM,对CD47的亲合力为59.5 nM)。同时为了增加抗体的药效,该抗体采用IgG1亚型,并且具有ADCP和ADCC等效应。PF-07257876对PD-L1具有更高的亲合力,因此使得抗体更多的聚集于肿瘤微环境中而不是外周血。双抗对CD47有较低的亲合力使得抗体具有更好的安全性,从而增加抗体治疗的窗口《辉瑞发表CD47/PD-L1双抗作用机制》。
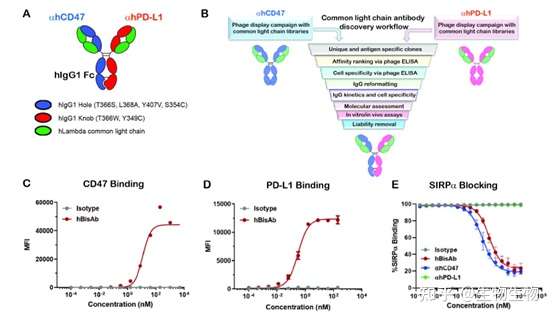
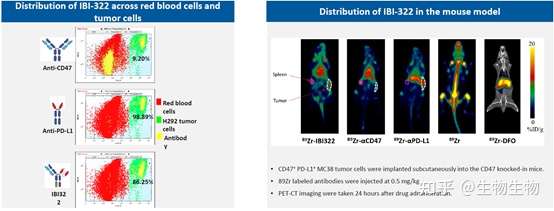
信达生物的IBI322同样是靶向CD47/PD-L1双特异抗体,其主要是通过抗体的结合价数调节对两个靶点的结合能力,该双抗采用1+2的形式,其中一个结合位点靶向CD47,另外两个结合位点靶向PD-L1,从而增加抗体在肿瘤中的分配,最终达到增加安全性的目的。
而对于SIRPα融合蛋白+抗体的双功能抗体,因为多数抗体与抗原的亲合力高于融合与其受体的亲合力;另外如果选择SIRPα V2D1融合,因其不和红细胞表面的CD47结合,因此理论上会比较安全,不用刻意的进行相对亲合力调整设计。
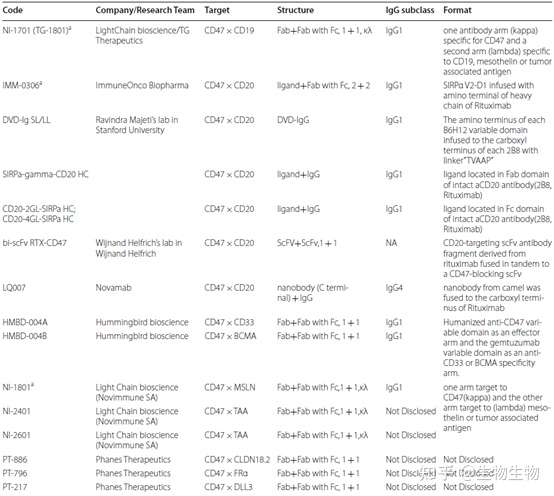
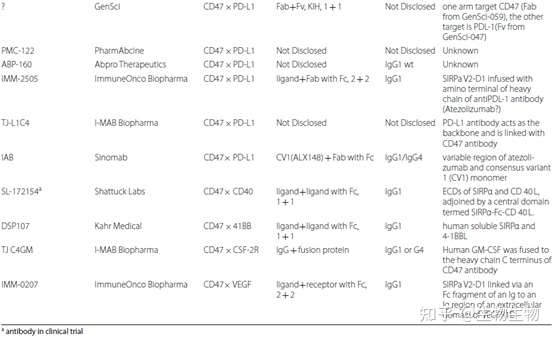
双特异抗体开发管线

5
细胞疗法
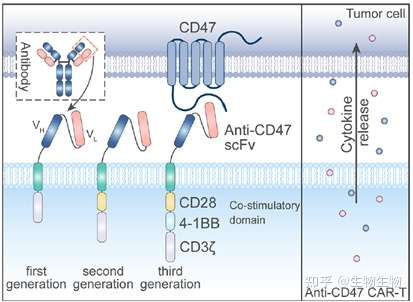
CAR-T细胞疗法,除了需要对靶向CD47的抗体进行设计,降低对红细胞表面的CD47的结合外,还需要对内部的激活元件进行设计,以更好的激活T细胞活性。目前CD47的CAR-T疗法都在临床研究中。
6
总结
目前主要有以下几种方法降低CD47- SIRPα相关药物的风险:
1)逐渐增加药物剂量,如Hu5F9-G4使用改良的给药方案,先给患者1 mg/kg的启动剂量(Priming dose)来触发体内老化红细胞的清除,虽然会导致暂时性轻度贫血,但同时可以刺激网织红细胞成熟分化产生新鲜的年轻红细胞。这些新生的红细胞表面表达“吃我”信号较低,对CD47抗体介导的吞噬作用不太敏感,因此可以承受后续Hu5F9 30 mg/kg的较高治疗剂量;
2)根据红细胞和癌细胞CD47构象及修饰不同,针对性筛选不结合红细胞表面CD47的抗体,如天境生物的TJC4等;
3)开发抗SIRPα抗体,与CD47的广泛表达不同,SIRPα的表达普较窄(多数位于骨髓瘤细胞上),因此SIRPα抗体不会与红细胞结合,理论上有较好的安全性;
4)除去Fc的相关效应功能或利用无功能的IgG亚型。对于靶向CD47的抗体,去除Fc的相关效应功能可以进一步提高安全性;
5)开发双特异抗体:双特异抗体中将结合CD47或者SIRPα的结构域的亲合力降低(低于另外一个靶点的亲合力),从而使得抗体在目标细胞上聚集,减少抗体对红细胞等细胞的结合,从而增加安全性,提高治疗窗口;
6)开发SIRPα融合蛋白:目前多数的SIRPα融合蛋白利用V2D1结构域,因为该结构域不结合红细胞表面的CD47,因此相对安全;
7)开发条件激活性抗体:如天演药业的CD47 SAFEbody,该抗体理论上在肿瘤微环境中利用肿瘤微环境中的特异酶酶切激活,从而可以避免On-target off-tumor效应。
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
卡梅德生物拥有成熟的四大核心技术服务平台:
1、稳定细胞系筛选与基础分子生物学平台;
2、抗体工程技术平台;
3、蛋白服务平台;
4、噬菌体展示技术服务平台;
我们成功研发了众多用于科学研究以及新药发现的重组蛋白、抗体、抗体药物靶点蛋白、工业酶、诊断原料等相关试剂,竭诚为您提供服务。

