卡梅德生物科技(天津)有限公司
6 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
卡梅德生物科技(天津)有限公司
入驻年限:6 年
- 联系人:
卡梅德-小智
- 所在地区:
天津 武清区
- 业务范围:
抗体、技术服务、体外诊断、原辅料包材、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
![科研级Tefibazumab(替非组单抗) Anti-Fibrin-binding Surface Epitope Clumping Factor A重组抗体 Fibrin-binding surface epitope clumping factor A[Staphylococcus aureus]参照抗体](https://img1.dxycdn.com/p/s14/2025/0725/806/0044791190482468491.jpg!wh200)
科研级Tefibazumab(替非组单抗) Anti-Fibrin-binding Surface Epitope Clumping Factor A重组抗体 Fibrin-binding surface epitope clumping factor A[Staphylococcus aureus]参照抗体
品牌:卡梅德/KMD Bioscience
¥500 - 3200
咨询
科研级Vedolizumab(维多组单抗) Anti-ITGA4 & ITGB7重组抗体 ITGA4 & ITGB7参照抗体
品牌:卡梅德/KMD Bioscience
¥500 - 3200
咨询技术资料/正文
SDS-PAGE跑胶总出问题?这篇“避坑指南”帮你搞定!
91 人阅读发布时间:2026-03-10 18:24
一.SDS-聚丙烯酰胺凝胶电泳
SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE,Sodium Dodecyl Sulfate Polyacrylamide Gel Electrophoresis)是蛋白质分析中最常用、最核心的技术之一。SDS-PAGE的原理离不开它的三个组分,分别是SDS、聚丙烯酰胺凝胶、还原剂(β-巯基乙醇或DTT)。
1. SDS
SDS是一种阴离子去垢剂,它能与蛋白质的疏水区域结合,以大约每两个氨基酸结合一个SDS分子的比例包裹蛋白质,使其携带大量的负电荷,这种电荷量远远超过蛋白质原本自身的电荷,使得所有蛋白质原本的等电点差异被掩盖,最终都携带相同密度的负电荷,除此之外,SDS能破坏蛋白质的氢键和疏水作用,使蛋白质从折叠状态伸展成直线状的棒状结构。
2. 聚丙烯酰胺凝胶
聚丙烯酰胺凝胶是一种人工合成的凝胶,由丙烯酰胺和交联剂甲叉双丙烯酰胺聚合而成。通过调整丙烯酰胺的浓度,可以控制凝胶孔径的大小,当蛋白质在电场中向正极(阳极)移动时,它们必须穿过凝胶的孔隙,分子量小的蛋白质体积小,在孔隙中穿行速度快;分子量大的蛋白质体积大,容易被凝胶孔隙卡住,移动速度相对较慢,这种差异使得在电泳过程中不同分子量的蛋白被分离开。
3. 还原剂(β-巯基乙醇或DTT)
通常在样品缓冲液中会加入β-巯基乙醇或DTT,使得样品处理过程中蛋白质中的二硫键被断裂,将多亚基蛋白彻底拆解成单独的线性肽链,这样最终跑出来的条带位置反映的是单个亚基的分子量。如果样品缓冲液中不加入还原剂,蛋白还存在二级结构使得蛋白结构更紧凑,在电泳过程中的迁移速度会快一些,从而使得跑出的条带位置会相对靠下一些。
二.SDS-聚丙烯酰胺凝胶电泳实验方案
1. 变性胶和非变性胶的选择
•变性胶
(1)纯度检测(最常用):比如做完镍柱纯化(His标签纯化)后,想知道洗脱液里到底有没有目标蛋白,以及有没有杂蛋白,变性胶就可以清晰展示各个组分的条带。
(2)分子量测定:验证表达的蛋白大小是否正确(比如预测是50kDa,跑出来确实是50kDa附近)。由于蛋白被完全线性化,分子量的估算相对准确。
(3)表达量分析:比较诱导前和诱导后,或者不同克隆之间的表达量高低。
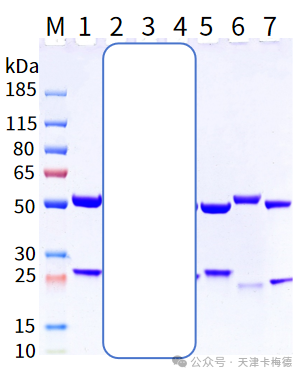
图1:IgG抗体鉴定-变性胶图
•非变性胶
(1)检测蛋白活性:如果你准备跑胶后进行酶活性染色(比如某个酶能分解底物产生颜色),就必须用非变性胶,因为只有保持天然构象的蛋白才有活性。
(2)分析蛋白复合物组成:想知道某个蛋白在天然状态下是单体、二聚体还是多聚体的形式,或者它是否与其他亚基结合成了复合物,这时应选用非变性胶。
(3)分析电荷异构体:有些蛋白由于翻译后修饰的不同(如磷酸化),带有不同的电荷。在非变性胶中,即使分子量相同,因为电荷不同,它们也会跑出不同的位置。
(4)脂蛋白或膜蛋白复合物分析:某些需要脂质环境维持稳定的蛋白复合物,只能在非变性条件下保持完整。
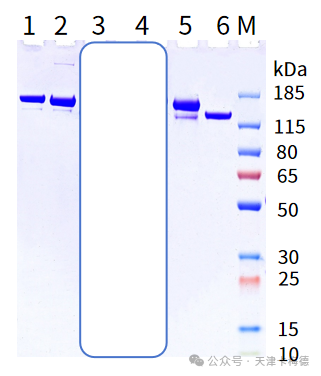
图2:IgG抗体鉴定-非变性胶图
2. 分离胶浓度的选择
|
分离胶浓度 |
最佳的分离范围 (kDa) |
适用场景举例 |
|
6% - 8% |
50 - 200 (甚至更大) |
大分子量蛋白:比如哺乳动物细胞表达的膜蛋白复合物、肌球蛋白(200 kDa)、或者你需要检测蛋白是否形成二聚体或多聚体的情况。 |
|
10% |
20 - 80 |
最常用的通用浓度:适用于大多数纯化后的重组蛋白。比如许多细胞因子(15-30 kDa)、抗体轻链(25 kDa)、单链抗体(~30 kDa)、以及大部分信号传导蛋白。 |
|
12% |
15 - 50 |
小蛋白的良好分离:当你的目标蛋白小于30 kDa时,用10%的胶可能会发现它跑得太快,条带不够锐利,甚至跑在最前沿的染料处。换成12%会让它慢下来,看得更清楚。 |
|
15% |
< 20 |
多肽或极小蛋白:用于分离像胰岛素、抗菌肽、或者小分子量的标签蛋白(如6xHis tag本身太小,通常看连接His的蛋白)。 |
|
4-20% 梯度胶 |
宽范围 (10 - 200) |
复杂样品全景分析:比如全细胞裂解液、血清样品。梯度胶结合了低浓度和高浓度的优势,大蛋白留在上方,小蛋白留在下方,都能得到分离。 |
三.SDS-聚丙烯酰胺凝胶电泳流程
1. SDS-聚丙烯酰胺凝胶制备
(1)组装胶板及制胶架,并进行验证其是否漏水,如漏水需调整胶板的组装,直到不漏水后方可进行后续步骤。
(2)制备下层分离胶:根据不同浓度凝胶配比进行凝胶溶液的调配,加入一定比例的促凝剂混匀并用移液器将凝胶溶液加入到胶板孔隙中,用自来水或酒精缓慢加到分离胶的上层进行液封。
(3)制备上层浓缩胶:将液封的自来水或酒精弃掉并用吸水纸擦拭干净,将配制好的浓缩胶加入胶板孔隙并轻轻插入梳子,胶板凝固过程中不要晃动配胶架,防止出现孔隙。
2. 样品处理
将蛋白样品与适量上样缓冲液混合(缓冲液中含有SDS/还原剂/甘油/溴酚蓝),在100°C金属浴或水浴中加热5-10分钟;如果是做非变性胶(Native-PAGE),这一步骤要省略,且缓冲液中不能有SDS和还原剂。
3. 上样并进行电泳
(1)将制好的凝胶板安装在电泳电极芯上,放入电泳槽。
(2)内槽倒满新鲜的SDS电泳缓冲液(含Tris、甘氨酸、SDS),外槽可倒部分回收的缓冲液。
(3)轻轻拔掉梳子,观察孔道是否垂直整齐,用注射器或移液枪吹洗孔道,去除未聚合的丙烯酰胺碎片。
(4)用细长的移液枪头或专用上样吸头,将处理好的样品缓慢加入孔底,加样速度要稳,避免样品冲出孔外。
(5)盖上盖子,连接电源(红对红,黑对黑),跑浓缩胶阶段通常用80V恒压,此时样品在浓缩胶中被压成一条细线;当溴酚蓝前沿进入分离胶并压缩成一条直线后,可将电压调至120-150V恒压;当溴酚蓝染料迁移至凝胶底部边缘时,关闭电源。
4.染色与脱色
(1)剥胶:取出玻璃板,用撬板轻轻分开短玻璃板。切去浓缩胶,将分离胶放入染色盒中。
(2)染色:加入考马斯亮蓝R-250染色液(通常溶于甲醇/乙酸溶液),确保覆盖凝胶,在摇床上缓慢摇晃30-60分钟(或微波炉加热10-20秒加速,但需防爆沸)。
(3)脱色:倒掉染色液(可回收使用多次),加入脱色液(通常是甲醇/乙酸/水混合液),在摇床上摇晃,期间更换脱色液几次,直到背景变透明,蓝色蛋白条带清晰可见。
卡梅德生物可以提供基础的分子生物学实验,包括SDS-PAGE验证、Western Blot检测,ELISA检测等,除此之外还可以提供以此为基础的蛋白表达及功能验证服务,蛋白互作检测等多类型服务,为众多科研学者保驾护航。
引用:
[1] Matsumoto H, Haniu H, Komori N. Determination of Protein Molecular Weights on SDS-PAGE. Methods Mol Biol. 2019;1855:101-105.
[2] Brunelle JL, Green R. One-dimensional SDS-polyacrylamide gel electrophoresis (1D SDS-PAGE). Methods Enzymol. 2014;541:151-9.
[3] Kielkopf CL, Bauer W, Urbatsch IL. Sodium Dodecyl Sulfate-Polyacrylamide Gel Electrophoresis of Proteins. Cold Spring Harb Protoc. 2021 Dec 1;2021(12).

